Učivo
Chemie
Galvanický článek
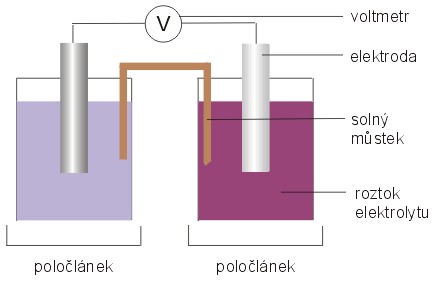
Galvanické články představují zdroj elektrické energie. Každý článek se skládá ze dvou poločlánků, což může být kov (elektroda) ponořený do roztoku jeho soli (elektrolytu). Pokud poločlánky mezi sebou vodivě propojíme, soustavou prochází elektrický proud a můžeme naměřit elektrické napětí.Napětí galvanického článku se vypočítá jako standardní redoxní potenciál katody mínus standardní redoxní potenciál anody a je vždy kladné.
E°(článek) = E°(katoda) − E°(anoda).
Jako katoda slouží kov, který je nejvíce ušlechtilý. Nikl tedy musí sloužit jako katoda. Anoda bude vyrobena z hliníku, který má nejnižší potenciál.
E°(článek) = -0,23-(-1,66) = 1,43V